हेस का स्थिर ऊष्मा योग नियम
यदि एक ही रासायनिक परिवर्तन एक या अधिक विधियों से, एक या अधिक पदों में पूर्ण किया जाये, तो पूर्ण परिवर्तन में उत्पन्न या शोषित ऊष्मा समान होती है। चाहे परिवर्तन किसी भी विधि से पूर्ण किया गया हो।
उदाहरणार्थ-
C(s) + O2(g) → CO2(g) + 94 kcal
इस अभिक्रिया को दो पदों में करने पर-
C(s) +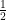 O2 (g) → CO(g)+ 264 kcal
O2 (g) → CO(g)+ 264 kcal
CO(g) +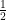 O2(g) → CO2(g) + 67.6 kcal
O2(g) → CO2(g) + 67.6 kcal
इन दोनों समीकरणों को जोड़ने पर-
C(s) +O2(g) → CO2(g)+ 94 kcal
इस प्रकार प्रत्येक दशा में एक मोल कार्बन के दहन से 94kcal ऊष्मा उत्सर्जित होती है। यह तथ्य हेस के नियम की पुष्टि करता है।